抗体药物科普(单抗、双抗、ADC)
抗体药物是基于免疫系统抗体分子设计的生物药,能精准靶向病变细胞或分子,具有特异性强、副作用小的特点,已成为肿瘤、自身免疫病等领域的主流治疗药物。以下是单抗、双抗、ADC 三类核心抗体药物的详细解析:
一、 单克隆抗体(单抗,Monoclonal Antibody, mAb)
知禾泰克 重组人源化抗人cd3单克隆抗体(图片来自网络)
1. 核心定义
由单一 B 细胞克隆产生的、针对单一抗原表位的同源抗体,结构与人体天然抗体(IgG 为主)高度相似。
2. 作用机制
靶向结合:特异性识别并结合靶抗原(如肿瘤细胞表面的 HER2、PD-1/PD-L1)。
效应功能:直接阻断靶分子的信号通路(如曲妥珠单抗阻断 HER2 信号,抑制乳腺癌细胞增殖);激活免疫系统(如 PD-1 单抗解除免疫抑制,让 T 细胞攻击肿瘤);介导抗体依赖的细胞毒性(ADCC)、补体依赖的细胞毒性(CDC),直接杀伤靶细胞。
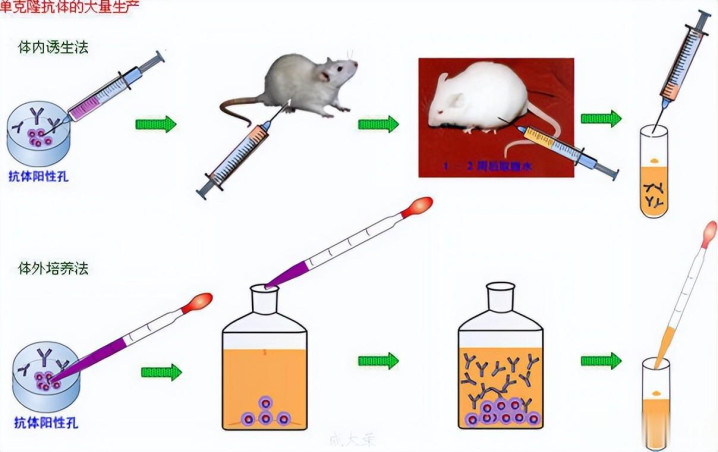
3. 典型药物与应用
靶点
药物名称
适应症
HER2
曲妥珠单抗
乳腺癌、胃癌
PD-1
帕博利珠单抗
黑色素瘤、非小细胞肺癌
TNF-α
阿达木单抗
类风湿关节炎、银屑病
4. 优缺点
优点:特异性高、疗效明确、安全性好;
缺点:仅靶向单一抗原,对异质性强的肿瘤(如晚期肺癌)疗效有限;部分药物存在免疫逃逸风险。
二、 双特异性抗体(双抗,Bispecific Antibody, BsAb)
1. 核心定义
通过基因工程技术制备的、能同时结合两个不同抗原或表位的抗体分子,可连接免疫细胞与靶细胞,或阻断两种不同的致病通路。
2. 核心设计思路
常见结构为 “双臂” 设计:一条臂靶向肿瘤细胞表面抗原(如 CD19、HER2),另一条臂靶向免疫细胞表面受体(如 CD3,T 细胞表面标志),形成 “免疫细胞 - 双抗 - 肿瘤细胞” 的三元复合物。
3. 作用机制
桥接效应:将 T 细胞、NK 细胞等免疫细胞直接招募到肿瘤细胞附近,激活免疫细胞的杀伤功能;
双靶点阻断:同时阻断两个独立的信号通路(如 EGFR 和 c-Met),避免单一靶点阻断后的耐药。
4. 典型药物与应用
靶点组合
药物名称
适应症
CD3/CD19
博纳吐单抗
急性淋巴细胞白血病
CD3/HER2
帕妥珠双抗
晚期 HER2 阳性乳腺癌
VEGF/ANG2
雷珠双抗
湿性年龄相关性黄斑变性
5. 优缺点
优点:克服单抗的单靶点局限,疗效更强;可实现 “精准制导” 的免疫杀伤,降低脱靶毒性;
缺点:结构复杂、制备工艺难度高、生产成本高;部分双抗可能引发细胞因子风暴(如 CD3 靶向双抗)。
三、 抗体药物偶联物(抗体偶联药物,Antibody-Drug Conjugate, ADC)
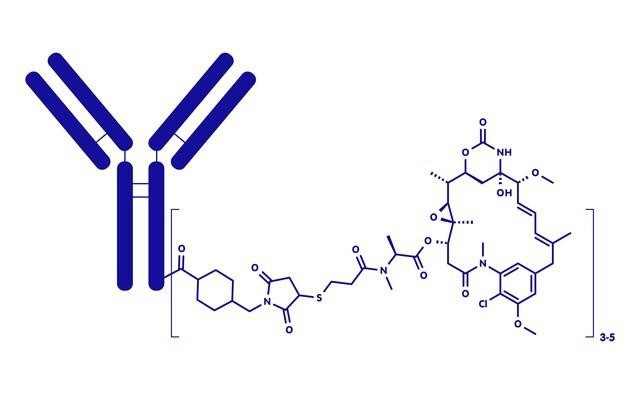
ADC药物举例
1. 核心定义
由 ** 单克隆抗体、细胞毒性药物(payload)、连接子(linker)** 三部分组成的 “生物导弹”:抗体作为导航系统靶向肿瘤细胞,连接子将抗体与毒素连接,毒素进入细胞后发挥杀伤作用。
ADC核心:靶向递送化疗毒素。
2. 核心设计要求
抗体:高特异性识别肿瘤细胞表面抗原(如 HER2、Trop-2),确保靶向性;
连接子:需具备 “肿瘤特异性裂解” 特性 —— 在血液循环中稳定,进入肿瘤细胞后(经溶酶体酶解或 pH 触发)释放毒素;
毒素:高效细胞毒性药物(如微管抑制剂、拓扑异构酶抑制剂),杀伤能力是传统化疗药的 10-100 倍。
3. 作用机制
抗体与肿瘤细胞表面抗原结合;
肿瘤细胞通过内吞作用将 ADC 摄入细胞内;
溶酶体降解抗体,连接子裂解释放毒素;
毒素干扰肿瘤细胞的 DNA 复制或微管组装,诱导细胞凋亡。
4. 典型药物与应用
靶点
药物名称
适应症
HER2
恩美曲妥珠单抗
晚期 HER2 阳性乳腺癌
Trop-2
戈沙妥珠单抗
三阴乳腺癌、尿路上皮癌
CD30
维布妥昔单抗
霍奇金淋巴瘤
5. 优缺点
优点:兼具抗体的靶向性和化疗药的杀伤性,疗效显著优于传统化疗和单抗;对多药耐药肿瘤仍有效;
缺点:连接子稳定性不足可能导致脱靶毒性(如骨髓抑制);部分 ADC 存在耐药性(如抗原丢失);制备工艺复杂,价格昂贵。
四、 三类抗体药物核心对比
特性
单抗
双抗
ADC
靶点数量
1 个
2 个
1 个
核心功能
靶向阻断 / 免疫激活
免疫桥接 / 双通路阻断
靶向递送化疗毒素
杀伤方式
免疫介导 / 直接阻断
免疫细胞介导杀伤
毒素诱导细胞凋亡
研发难度
低
中 - 高
中 - 高
副作用
较轻(免疫反应为主)
可能引发细胞因子风暴
骨髓抑制、消化道反应
(本文内容仅供科普知识所用,与医疗无关)


